
Un panel de expertos de la FDA recomienda no aprobar una vacuna de refuerzo contra el coronavirus en Estados Unidos
Una abrumadora mayoría de científicos considera que no hay evidencia suficiente para que los adultos sanos reciban una tercera dosis.
Internacionales18/09/2021 Editor
Editor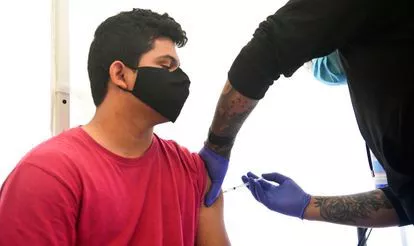
Un panel de expertos de la agencia reguladora de medicamentos en Estados Unidos (FDA, por sus filas en inglés) ha recomendado este viernes no aprobar una inyección de refuerzo de la vacuna de Pfizer-BioNTech contra el coronavirus a los mayores de 16 años. El comité, que parecía bastante dividido durante el debate, decidió por 16 votos en contra y solo 3 a favor de aprobar la tercera dosis. La FDA no está obligada a seguir las recomendaciones del comité asesor, pero suele seguirlas. La decisión trunca los planes de la Administración de Joe Biden que esperaba poner en marcha las vacunas de refuerzo para atajar la propagación del virus debido a la variante delta.
La discusión de los expertos independientes se centró en aclarar si la caída en la efectividad de las vacunas puede llevar a un aumento de los casos graves de covid entre los inoculados. La diversa interpretación de los datos fue lo que marcó del debate que se prolongó durante toda la mañana. “Sabemos que puede haber diferentes opiniones al interpretar los datos”, sostuvo el doctor Peter Marks, director del Centro de Evaluación e Investigación Biológica de la FDA, quien reconoció que “son complejos y están en evolución”. La información presentada por la doctora Sara Oliver, de los Centros para el Control y Prevención de Enfermedades (CDC, por sus siglas en inglés), reveló que las dos dosis de la vacuna siguen evitando la covid grave, incluso en los mayores de 75 años. Por su parte, los expertos israelíes, apoyados en su propia experiencia, aseguraron que la dosis de refuerzo redujo drásticamente los casos graves provocados por la variante delta.
Israel aprobó en julio la tercera inyección de Pfizer-BioNTech. Un estudio que analizó los resultados de esa decisión arrojó que los mayores de 60 años que recibieron una dosis de refuerzo tenían un riesgo 11 veces menor de infectarse que las personas a las que no se les inoculó el tercer pinchazo, según la investigación publicada el miércoles en el New England Journal of Medicine. Si bien el debate de este viernes en EE UU abordaba solo a Pfizer-BioNTech, la decisión era mayúscula, ya que definió el recorrido del resto de las vacunas aprobadas en la potencia mundial.
Los principales funcionarios federales de salud de EE UU, incluido el doctor Anthony Fauci, asesor médico en jefe del presidente Biden, llevan semanas alertando de que la inmunidad decae entre los inoculados con la pauta completa y que ya hay indicios de un retroceso en la eficacia para proteger a los inoculados en los casos graves, lo que puede derivar en un aumento de las hospitalizaciones. De las tres vacunas disponibles en EE UU, Moderna es la más efectiva (93%) para evitar que las personas acaben en el hospital, según un estudio de los CDC publicado este viernes, aunque el único fármaco que cuenta con la aprobación completa de la agencia de medicamentos es Pfizer-BioNTech.
A pesar de que todavía existe la mínima posibilidad de que la FDA apruebe la dosis de refuerzo, la agencia no es la que zanja el tema. Los asesores de los CDC se reunirán el próximo miércoles y jueves para definir quiénes y cuándo podrán recibir una tercera ronda de inyecciones —en caso de que la agencia de los medicamentos lo apruebe—. A mediados de agosto, Biden anunció un plan para ofrecer la dosis de refuerzo a partir del 20 de septiembre a los inoculados con Pfizer-BioNTech y Moderna. Varios expertos en salud consideraron que el movimiento era prematuro. Además, el mandatario hizo el anuncio públicamente antes de que la FDA tomara una decisión sobre si era conveniente basándose en la evidencia disponible.
Biden aseguró que los vacunados podrían inocularse por tercera vez ocho meses después de haber recibido la segunda dosis, pero la farmacéutica Pfizer-BioNTech le solicitó a la FDA que el plazo fuera solo de seis meses. La opción de aprobar el refuerzo de Moderna se ha retrasado.
Desde el 13 de agosto los pacientes inmunodeprimidos pueden recibir una tercera dosis de Pfizer y Moderna en EE UU. La Organización Mundial de la Salud (OMS, por sus siglas en inglés) se ha opuesto a que los países más ricos administren una tercera dosis cuando los más pobres aún no cuentan con vacunas suficientes para inmunizar por primera vez a su población elegible. Dos importantes revisores de vacunas de la FDA firmaron este lunes junto a un grupo de científicos internacionales un artículo en The Lancet, donde rechazaban la necesidad de refuerzos en personas sanas debido a la falta de evidencias. Ambos van a renunciar a la agencia reguladora. Una de ellas, la doctora Marian Gruber, intervino esta mañana en el panel: “Todas mis acciones y decisiones a lo largo de mis 32 años de carrera en la FDA se han basado en la ciencia”.


Triple femicidio: la Justicia de Perú aprobó la extradición de "Pequeño J "a la Argentina
Se trata del principal acusado por el triple crimen ocurrido en Florencio Varela. Fue detenido en septiembre del año pasado en Lima luego de haberse fugado del conurbano bonaerense.

Amnistía en Venezuela: cautela y reclamos de libertad para los argentinos detenidos
Tras el anuncio de la presidenta encargada Delcy Rodríguez, las familias del gendarme Nahuel Gallo y el abogado Germán Giuliani exigen que la medida se traduzca en hechos concretos.

Demandan a una clínica de fertilidad luego descubrir que su bebé no es genéticamente de ellos
El matrimonio realizó una prueba de AND y confirmó que la niña no tiene vínculo biológico con ellos y temen que los padres genéticos reclamen su custodia.

Gustavo Petro aseguró que "Jesús hizo el amor" y la Iglesia lo consideró una falta de respecto
El presidente colombiano sugirió que pudo haber sostenido una relación con María Magdalena. Esto desató una respuesta inmediata de las autoridades religiosas.

Australia vive una de las olas de calor más extremas de la historia
El país atraviesa un episodio climático extremo sin precedentes, con temperaturas que superaron los 49 grados, noches que no ofrecen alivio y récords históricos en distintas regiones. El fenómeno, impulsado por una “cúpula de calor” que bloquea el ingreso de aire frío, ya impacta en la salud, el ambiente y la actividad cotidiana, y es considerado por los expertos como uno de los más severos registrados.


Incendio forestal en Bovril: un avión hidrante y brigadistas de 5 ciudades combaten el fuego
Brigadistas de Paraná, Hasenkamp, María Grande, Bovril y Alcaraz trabajan sobre el fuego que afecta la zona de la Estancia El Durazno, cerca de Bovril aunque en jurisdicción del departamento Paraná.

Dos personas, un hombre y una mujer, fueron detenidos en el "marco de una investigación" por funcionarios policiales de la Cría 7ma. "en la zona Oeste de la ciudad".

Una persona perdió un dedo por palometas en el Río Paraná: hay una ciudad entrerriana en alerta
Un trabajador ribereño asistió a 46 bañistas y el hospital local atendió casos con lesiones severas, entre ellos uno de extrema gravedad.

Peajes sin efectivo: recuerdan que el 100% del cobro es electrónico y recomiendan usar TelePASE
Así lo informó Autovía del Mercosur en un comunicado difundido este martes, a raíz de confusiones de los usuarios. Señalaron que el uso del dispositivo electrónico es "más ágil y económico". En breve comenzará a funcionar el pago con tarjetas de débito y crédito.
.




